業務内容の紹介
業務内容の紹介
ご挨拶
再生医療・細胞治療の分野は近年加速度的に臨床応用が進んでいますが、実際に治療を受けられる患者さんは限られています。再生医療等推進部門は、研究者の先生方が開発した革新的な再生医療・細胞治療を、少しでも早く、一人でも多くの患者さんへ届けるために、実用化に向けたお手伝いをしています。厳しく管理された細胞プロセッシング室(Cell Processing Center: CPC)では、十分な教育訓練を受けたスタッフが、十分に検証されたルールに従い細胞や細胞製品を取り扱っており、高い品質の再生医療等製品・細胞治療薬を出荷できる体制を整えています。同時に、当部門のノウハウを生かし、既に承認された再生医療を北大病院で安全に実施するための支援も行っています。
これから再生医療・細胞治療の臨床応用を考えている研究者の先生方、治験を予定されている企業の方々、皆様のアイディアや技術をベッドサイドに届けるお手伝いをいたします。是非ご相談下さい。

沿革
| 前身となる高度先進医療支援センター内に 細胞プロセッシング室1ユニットを設立、 造血幹細胞移植用細胞の調製作業を開始 |
|
| 再生医療等製品の企業治験支援(製品の保管・調整業務)開始 | |
| 現在の場所に細胞プロセッシング室2ユニットを設立 | |
| 最初の開発プロジェクト「自家単核球/樹状細胞」(医師主導治験)の予備製造開始 | |
| 細胞プロセッシング室3ユニットを増設 PMDAによる施設・設備の実地調査の受審 臨床研究開発センター発足 「羊膜由来間葉系幹細胞」の予備製造開始(医師主導治験) |
|
| 再生医療安全確保法に基づく細胞培養加工施設の届出提出 「自家骨髄由来間葉系幹細胞」の予備製造開始(医師主導治験) |
|
| 「ドナー由来制御性T細胞」の予備製造開始(臨床研究) | |
| 「自家骨髄由来間葉系幹細胞」(医師主導治験)の第1例目の出荷 | |
| 新規再生医療等製品「自家骨髄由来間葉系幹細胞」の開発開始 | |
| 再生医療等製品「キムリア」の国内最初の施設認定取得、国内1例目の原料細胞出荷 |
表は横にスクロールしてご覧いただけます
組織構成
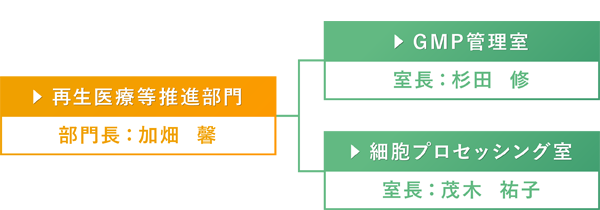
● スタッフ6名/共同研究員2名(2021年5月末現在)
● 職種:医師(1)、薬剤師(1)
● 学位:医学博士(1)、薬学博士(1)、工学博士(1)
● 資格:再生医療認定医(1)、臨床培養士(2)、細胞治療認定管理師(1)
● 職種:医師(1)、薬剤師(1)
● 学位:医学博士(1)、薬学博士(1)、工学博士(1)
● 資格:再生医療認定医(1)、臨床培養士(2)、細胞治療認定管理師(1)
再生医療等推進部門の業務
- 薬機法(医師主導治験)、再生医療法(臨床研究)による再生医療等製品の開発と製造
- ●製造業務
●品質試験、およびそのバリデーション
●製造手順書(標準書)、および概要書の作成支援
●外部委託先の選定・審査
●製造記録書の保存(10年、若しくは30年間)
●参考品の保存(10年、若しくは30年間)
- 企業治験支援(再生医療等製品)
- ●製品の保管・調製業務など
- コンサルテーション業務
- ●再生医療等製品開発に関する内容
●CPCの管理・維持に関する内容
- 診療支援
- ●造血幹細胞移植片の保管・調整業務、品質管理
●再生医療等製品の保管・調整業務
- CPCの管理・維持
- ●サニテーション、環境試験
●定期バリデーション
製造管理体制
再生医療等推進部門では、GMP(Good Manufacturing Practice)/ GCTP(Good Gene、Cellular、and Tissue-based Products Manufacturing Practice)を遵守した製造体制を構築し、高品質な再生医療等製品の製造に努めています。